
TORNE A PROTEÇÃO
NO SEU SUPERPODER
JARDIANCE® protege reduzindo o risco em doentes adultos com DRC*1,2, IC†3,4 e DT2 + DCVe‡5.

SABIA QUE A DRC ATUA COMO UM MULTIPLICADOR DE RISCO?6,7
As doenças cardíacas, renais e metabólicas estão interligadas!8

AJUDE A PROTEGER OS SEUS DOENTES COM JARDIANCE®
JARDIANCE® demonstrou diferentes benefícios para os seus doentes com DT2 + DCVe1
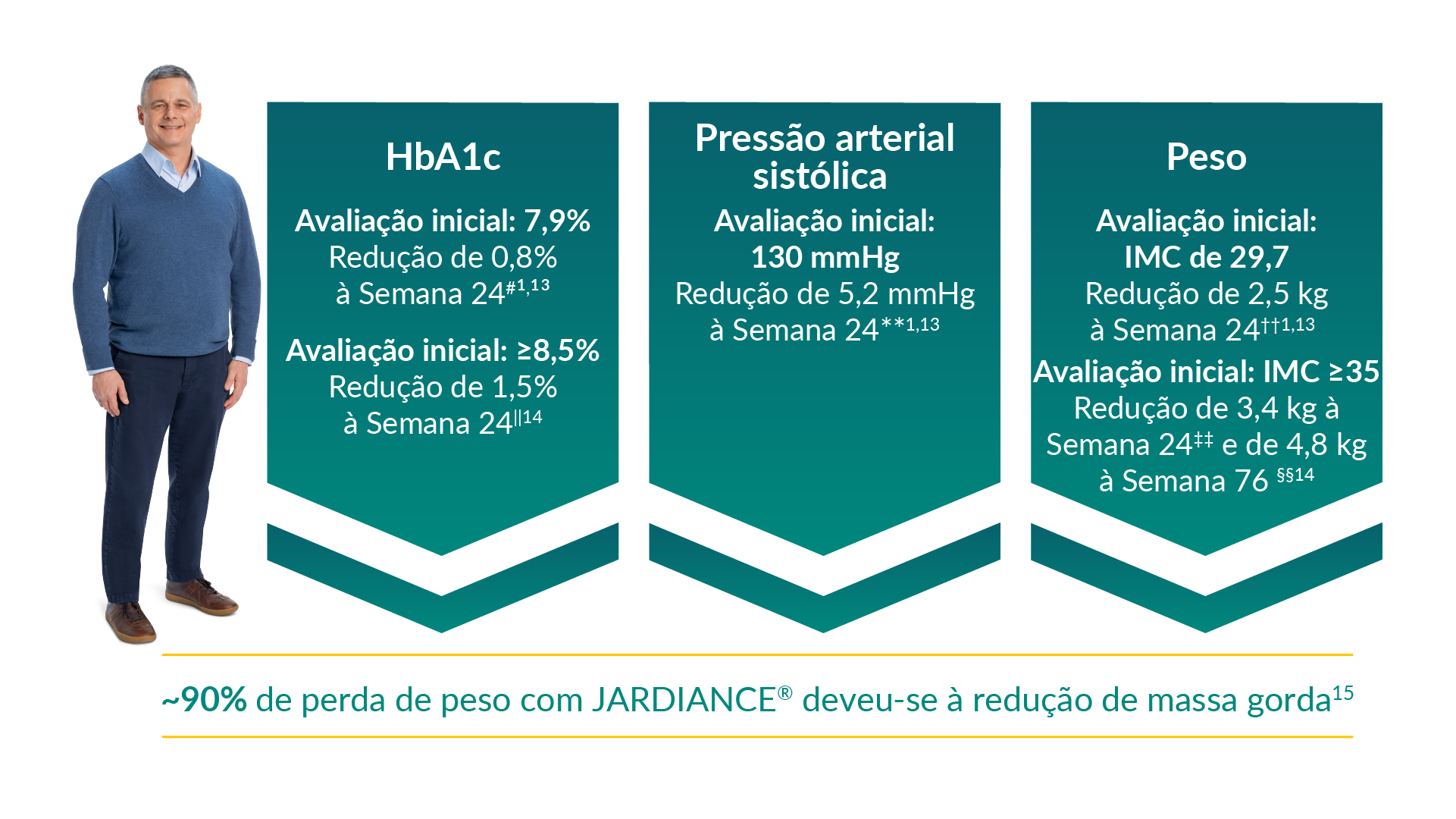
EM DOENTES ADULTOS COM DT2 + DCVe
Benefícios ao nível da HbA1c, da pressão arterial sistólica e peso¶1,13,14
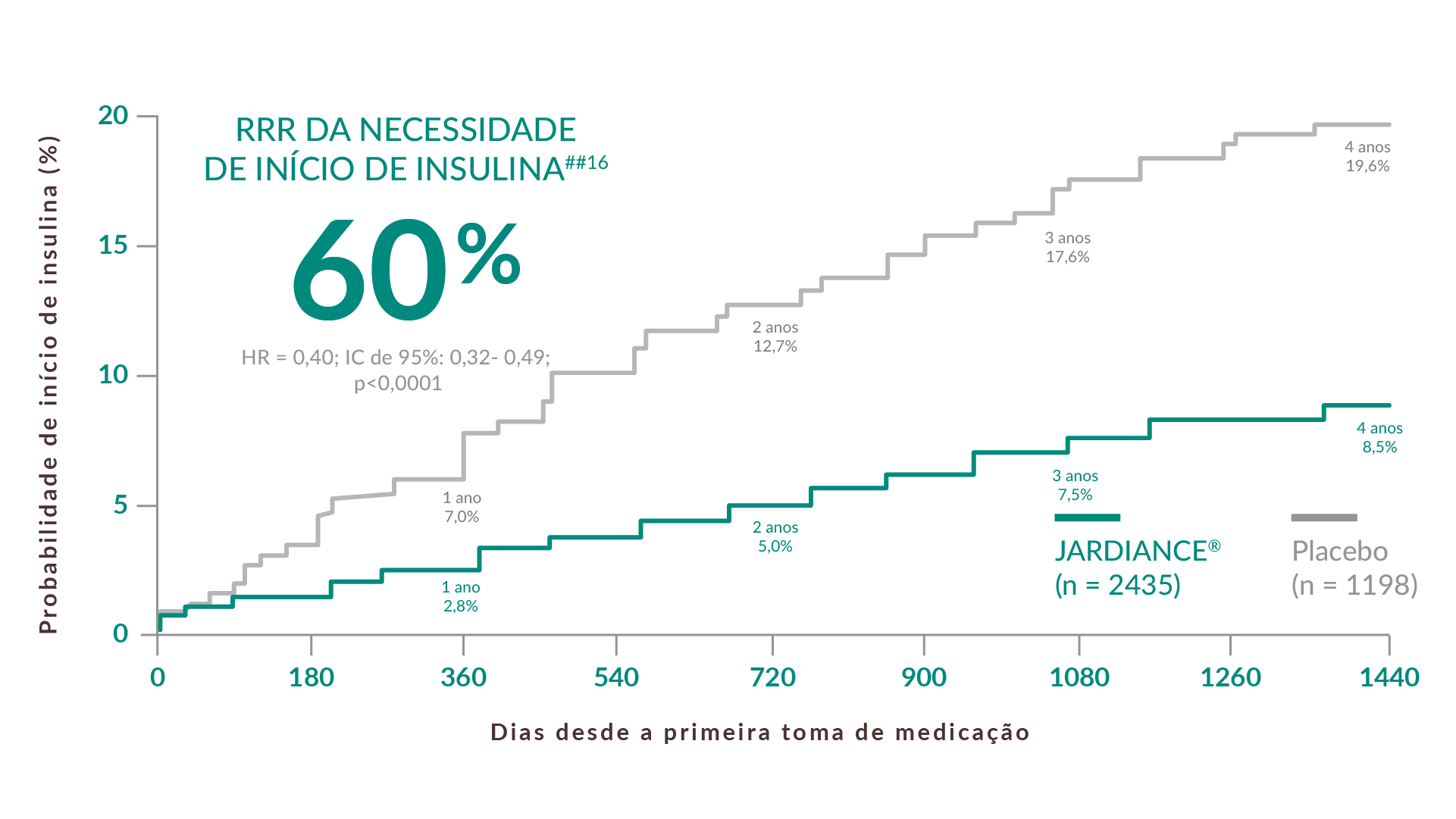
EM DOENTES COM DT2 + DCVe NÃO TRATADOS COM INSULINA§
60% de RRR da necessidade de início de insulina##16
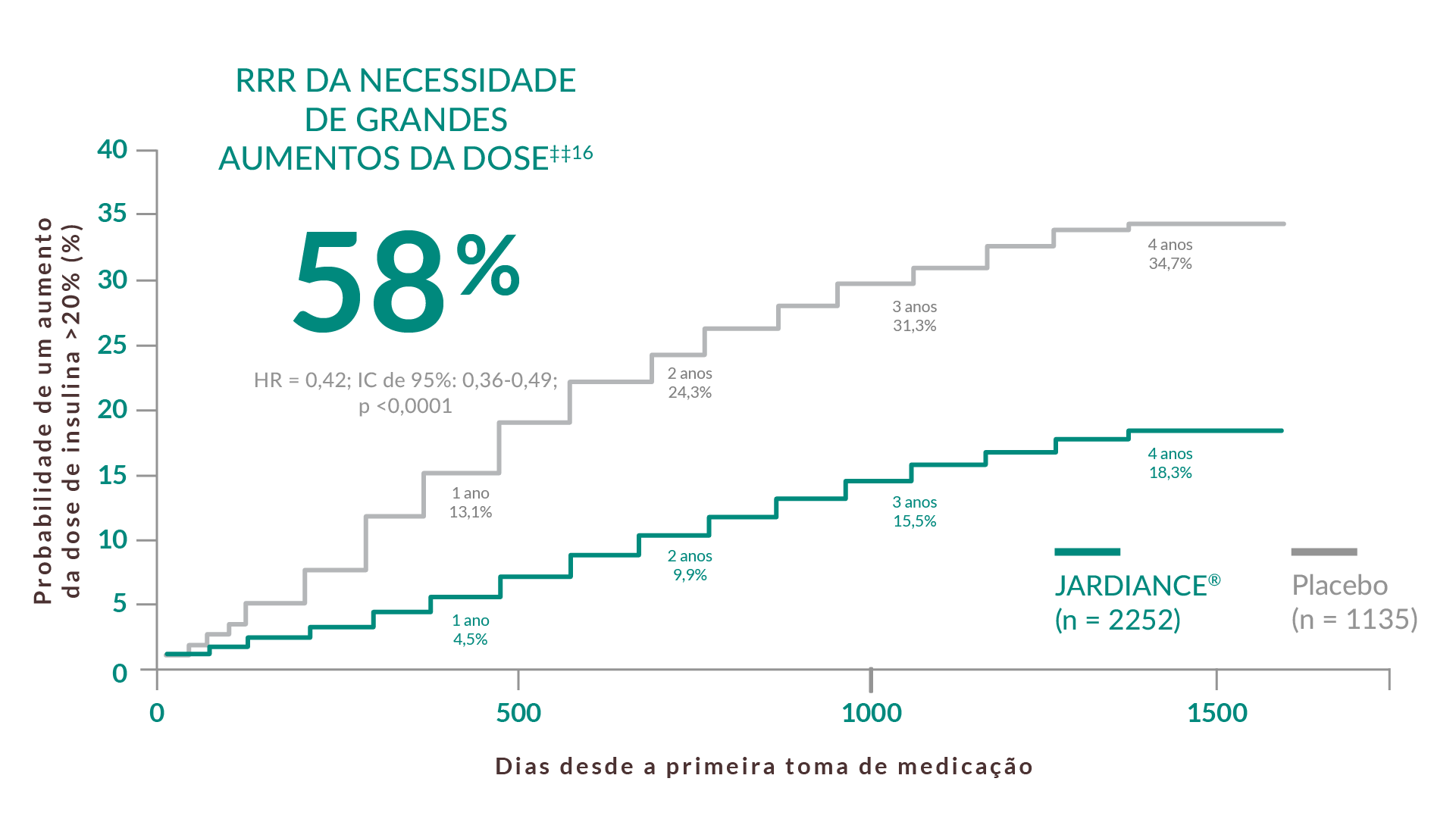
EM DOENTES COM DT2 + DCVe TRATADOS COM INSULINA§
58% de RRR de doses elevadas de insulina‡‡16
Indicações
JARDIANCE® está indicado para o tratamento de adultos e crianças com idade igual ou superior a 10 anos com diabetes mellitus tipo 2 insuficientemente controlados, como um adjuvante da dieta e do exercício
em monoterapia quando a metformina é considerada inapropriada devido à intolerância
em associação com outros medicamentos para o tratamento da diabetes
JARDIANCE® é indicado em adultos para o tratamento da insuficiência cardíaca crónica sintomática.
JARDIANCE® é indicado em adultos para o tratamento da doença renal crónica.
Notas de rodapé
-
*
No ensaio EMPA-KIDNEY, um estudo aleatorizado, de grupos paralelos, em dupla ocultação e controlado por placebo de 6609 doentes com DRC, foram avaliados os perfis de eficácia e segurança de JARDIANCE® 10 mg (n = 3304) em comparação com placebo (n = 3305). O endpoint primário no ensaio EMPA-KIDNEY foi um composto de morte CV ou progressão da doença renal definida como doença renal terminal (início de diálise de manutenção ou receção de um transplante renal), uma diminuição sustentada na TFGe para <10 ml/min/1,73 m2, uma diminuição sustentada na TFGe ≥40%, desde a avaliação inicial, ou morte por causas renais. Os doentes tratados com JARDIANCE® apresentaram 28% de RRR neste endpoint (HR = 0,72; IC de 95%: 0,64-0,82; p<0,001).2
-
†
No ensaio EMPEROR-Reduced, um estudo aleatorizado, em dupla ocultação, de grupos paralelos e controlado por placebo de 3730 doentes com ICFEr, foram avaliados os perfis de eficácia e segurança de JARDIANCE® 10 mg (n = 1863) em comparação com placebo (n = 1867). Os doentes eram adultos com insuficiência cardíaca crónica (classe NYHA II, III ou IV ) e fração de ejeção reduzida (FEVE ≤40%). O endpoint primário no ensaio EMPEROR-Reduced foi um composto de morte CV ou HIC, numa análise de tempo até ao primeiro acontecimento. Os doentes tratados com JARDIANCE® apresentaram 25% de RRR neste endpoint (HR = 0,75; IC de 95%: 0,65- 0,86; p<0,001). No ensaio EMPEROR-Preserved, um ensaio aleatorizado, em dupla ocultação, de grupos paralelos e controlado por placebo de 5988 doentes com ICFEp, foram avaliados os perfis de eficácia e segurança de JARDIANCE® 10 mg (n = 2997) em comparação com placebo (n = 2991). Os doentes eram adultos com insuficiência cardíaca crónica (classe NYHA II, III ou IV da ) e fração de ejeção preservada (FEVE >40%). O endpoint primário no ensaio EMPEROR-Preserved foi um composto de morte CV ou HIC, numa análise de tempo até ao primeiro acontecimento. Os doentes tratados com JARDIANCE® apresentaram 21% de RRR neste endpoint (HR = 0,79; IC de 95%: 0,69- 0,90; p<0,001).3,4
-
‡
O resultado composto primário do ensaio EMPA-REG OUTCOME® foi MACE de 3 critérios, constituído por morte CV, EM não fatal ou AVC não fatal, conforme analisado no grupo combinado de JARDIANCE® versus o grupo do placebo. Os doentes eram adultos com DT2 insuficientemente controlada e DAC, DAP, ou antecedentes de EM ou AVC. A RRR de 14% em MACE de 3 critérios (HR = 0,86; IC de 95%: 0,74- 0,99; p <0,001 para não inferioridade; p = 0,04 para superioridade) deveu-se a uma redução do risco de morte CV (HR = 0,62; IC de 95%: 0,49- 0,77).5
-
§
Doentes adultos com DT2 insuficientemente controlada e DAC, DAP ou antecedentes de EM ou AVC.1,5
-
¶
Num estudo de 24 semanas, em dupla ocultação, controlado por placebo, de 637 doentes com DT2, os perfis de eficácia e segurança de JARDIANCE® 10 mg (n = 217) e JARDIANCE® 25 mg (n = 213) como terapêutica combinada com metformina ≥1500 mg, foram avaliadas em comparação com placebo adicionado a metformina (n = 207). O endpoint primário foi a alteração média ajustada (EP), desde a avaliação inicial, da HbA1c (%); a perda de peso e a redução da pressão arterial foram os principais endpoints secundário e exploratório, respetivamente.13 JARDIANCE® não está indicado para a perda de peso nem para a redução da pressão arterial.1
-
#
Alterações médias ajustadas de –0,1% em relação ao valor de HbA1c basal de 7,9% para placebo (n = 207), –0,7% em relação ao valor basal de HbA1c de 7,9% para JARDIANCE® 10 mg (n = 217), e –0,8% em relação ao valor de HbA1c basal de 7,9% para JARDIANCE® 25 mg (n = 213), respetivamente. A diferença relativamente ao placebo (média ajustada) foi de -0,6% para JARDIANCE® 10 mg e 25 mg; p<0,001 em comparação com o placebo para ambas as doses.1,13
-
||
Numa análise de subgrupos, às 24 semanas, de doentes com valores na avaliação inicial ≥8,5%, as alterações médias ajustadas da HbA1c foram de –0,5% para o placebo (n = 50), –1,2% para o JARDIANCE® 10 mg (n = 57) e –1,5% para o JARDIANCE® 25 mg (n = 48). A diferença relativamente ao placebo (média ajustada) foi de –0,73% para JARDIANCE® 10 mg e de –1,0% para JARDIANCE® 25 mg. Os dados em falta foram imputados com recurso à última observação efetuada [tradução direta de: last observation carried forward (LOCF)].14
-
**
Alteração média ajustada da pressão arterial sistólica desde a avaliação inicial às 24 semanas: JARDIANCE® 10 mg: -4,5 mmHg (n=217) e JARDIANCE® 25 mg: -5,2 mmHg (n=213) vs. placebo: -0,4 mmHg (n=207).13
-
††
Alterações médias ajustadas de redução do peso corporal de –0,45 kg desde os 79,7 kg na avaliação inicial para o placebo (n = 207), –2,08 kg desde os 81,6 kg na avaliação inicial para o JARDIANCE® 10 mg (n = 217), e de –2,46 kg desde os 82,2 kg na avaliação inicial para o JARDIANCE® 25 mg (n = 213), respetivamente; p <0,0001 em comparação com placebo para ambas as doses.1,13
-
§§
Numa análise de subgrupos às 24 semanas de doentes com IMC na avaliação inicial ≥35, as alterações médias ajustadas do peso foram de –0,34 kg para o placebo (n = 29), –2,63 kg para o JARDIANCE® 10 mg (n = 33) e –3,35 kg para o JARDIANCE® 25 mg (n = 41). A diferença relativamente ao placebo (média ajustada) foi de –2,28 para o JARDIANCE® 10 mg e de –3,01 para o JARDIANCE® 25 mg.14
-
¶¶
Num ensaio de extensão em dupla ocultação, as alterações médias ajustadas do peso para doentes com avaliação inicial de IMC ≥35 na Semana 76 foram de 0,23 kg para o placebo (n = 29), –3,74 kg para JARDIANCE® 10 mg (n = 33) e –4,77 kg para JARDIANCE® 25 mg (n = 41). A diferença relativamente ao placebo (média ajustada) foi de –3,96 kg para o JARDIANCE® 10 mg e de –4,99 kg para o JARDIANCE® 25 mg. Os dados em falta foram imputados utilizando a abordagem LOCF.14
-
##
O resultado do início de insulina foi definido para ser mantido em ≥2 consultas consecutivas com ≥13 semanas de intervalo. Modelo de regressão de Cox ajustado à avaliação inicial da HbA1c, ao tempo decorrido desde o diagnóstico de DT2, ao IMC, à TFGe, à região geográfica e à fase de tratamento. Estimativas de Kaplan-Meier.16
-
‡‡
O aumento sustentado da dose de insulina foi definido como o tempo até ao primeiro aumento na dose total diária de insulina >20% relativamente à dose total diária de insulina na avaliação inicial, mantido durante pelo menos 2 consultas consecutivas com um mínimo de 13 semanas de intervalo, analisado em doentes tratados com insulina na avaliação inicial.16
-
CV = cardiovascular; DAC = doença arterial coronária; DAP = doença arterial periférica; DCVe = doença cardiovascular estabelecida; DRC = doença renal crónica; DT2 = diabetes tipo 2; EM = enfarte do miocárdio; EP = erro padrão da média; FEVE = fração de ejeção ventricular esquerda; IC = intervalo de confiança; IC = insuficiência cardíaca; ICFEp = insuficiência cardíaca com fração de ejeção preservada; ICFEr = insuficiência cardíaca com fração de ejeção reduzida; IMC = índice de massa corporal; MACE = acontecimentos cardiovasculares adversos graves; NNT = número necessário para tratar; NYHA = New York Heart Association (Associação de Cardiologia de Nova Iorque); PA = pressão arterial; PAS = pressão arterial sistólica; RRA = redução de risco absoluto; RRR = redução do risco relativo; TFGe = taxa de filtração glomerular estimada; TR = taxa de risco.
Bibliografia
-
RCM de Jardiance® (Abr/2025)
-
Herrington WG, Staplin N, Wanner C, et al. EMPA-KIDNEY Collaborative Group. Empagliflozin in patients with chronic kidney disease. N Engl J Med. 2023;388(2):117-127. (EMPA-KIDNEY results and the publication’s Supplementary Appendix.)
-
Packer M, Anker SD, Butler J, et al; EMPEROR-Reduced Trial Investigators Cardiovascular and renal outcomes with empagliflozin in heart failure. N Engl J Med. 2020;383(15):1413-1424. (EMPEROR-Reduced results and the publication’s Supplementary Appendix.)
-
Anker SD, Butler J, Filippatos G, et al; EMPEROR-Preserved Trial Investigators. Empagliflozin in heart failure with a preserved ejection fraction. N Engl J Med. 2021;385(16):1451-1461. (EMPEROR-Preserved results and the publication’s Supplementary Appendix.)
-
Zinman B, Wanner C, Lachin JM, et al; EMPA-REG OUTCOME Investigators. Empagliflozin, cardiovascular outcomes, and mortality in type 2 diabetes. N Engl J Med. 2015;373(22):2117-2128. (EMPA-REG OUTCOME® results and the publication’s Supplementary Appendix.)
-
GBD Chronic Kidney Disease Collaboration. Global, regional, and national burden of chronic kidney disease, 1990-2017: a systematic analysis for the Global Burden of Disease Study 2017. Lancet. 2020;395(10225):709-733.
-
Jankowski J, Floege J, Fliser D, Böhm N, Marx N. Cardiovascular disease in chronic kidney disease: pathophysiological insights and therapeutic options. Circulation. 2021;143(11):1157-1172.
-
Kalra S, Aydin H, Sahay M, et al. Cardiorenal syndrome in type 2 diabetes mellitus—rational use of sodium-glucose cotransporter-2 inhibitors. Eur Endocrinol. 2020;16(2):113-121.
-
McDonagh TA, Metra M, Adamo M, et al; ESC Scientific Document Group. 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2021;42(36):3599-3726.
-
Davies MJ, Aroda VR, Collins BS, et al. Management of hyperglycemia in type 2 diabetes, 2022: a consensus report by the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD). Diabetes Care. 2022;45(11):2753-2786.
-
Heidenreich PA, Bozkurt B, Aguilar D, et al. 2022 AHA/ACC/HFSA Guideline for the Management of Heart Failure: a report of the American College of Cardiology/American Heart Association Joint Committee on Clinical Practice Guidelines. J Am Acad Cardiol. 2022;79(17):e263-e421.
-
Kidney Disease: Improving Global Outcomes (KDIGO) CKD Work Group. KDIGO 2024 Clinical Practice Guideline for the Evaluation and Management of Chronic Kidney Disease. Kidney Int. 2024 Apr;105(4S):S117-S314.
-
Häring HU, Marker L, Seewaldt-Becker E, et al; EMPA-REG MET Trial Investigators. Empagliflozin as add-on to metformin in patients with type 2 diabetes: a 24-week, randomized, double-blind, placebo-controlled trial. Diabetes Care. 2014;37(6):1650-1659.
-
Inzucchi SE, Davies MJ, Khunti K, et al. Empagliflozin treatment effects across categories of baseline HbA1c, body weight, and blood pressure as an add-on to metformin in patients with type 2 diabetes. Diabetes Obes Metab. 2021;23(2):425-433
-
Ridderstrale M, Andersen KR, Zeller C, Kim G, Woerle HJ, Broedl UC; EMPA-REG H2H-SU Trial Investigators. Comparison of empagliflozin and glimepiride as add-on to metformin in patients with type 2 diabetes: a 104-week randomised, active-controlled, double-blind, phase 3 trial. Lancet Diabetes Endocrinol. 2014;2(9):691-700.
-
Vaduganathan M, Inzucchi SE, Sattar N, et al. Effects of empagliflozin on insulin initiation or intensification in patients with type 2 diabetes and cardiovascular disease: findings from the EMPA-REG OUTCOME trial. Diabetes Obes Metab. 2021;23(12):2775-2784.
-
McDonagh TA, Metra M, Adamo M, et al. 2023 Focused Update of the 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J. 2023 Oct 1;44(37):3627-3639. Erratum in: Eur Heart J. 2024 Jan 1;45(1):53.
EM DOENTES ADULTOS COM DT2 + DCVe§
39% de RRR de nefropatia¶1,3
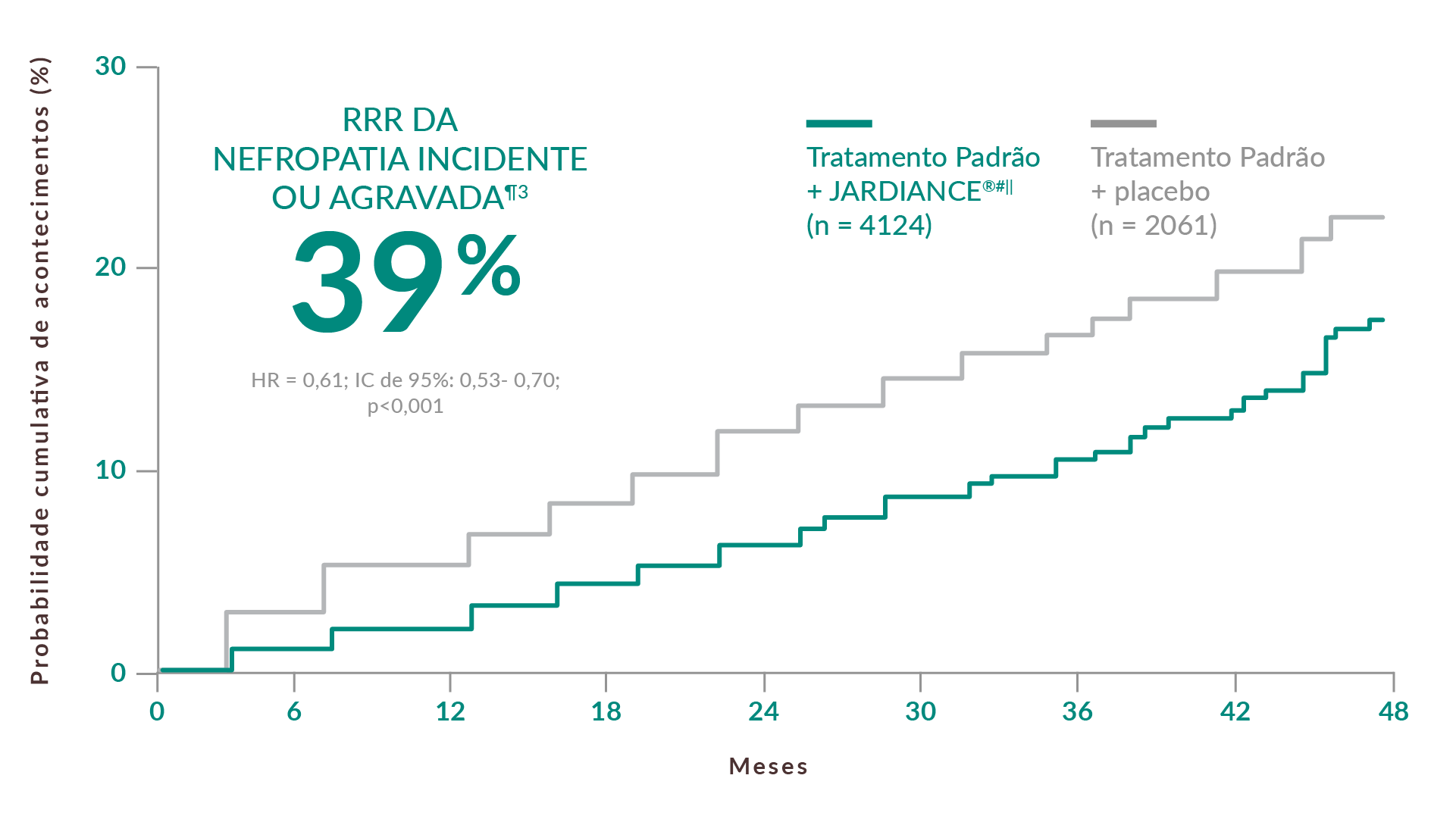
EM DOENTES ADULTOS COM DT2 + DCVe§
Abrandamento do declínio da função renal¶1,3
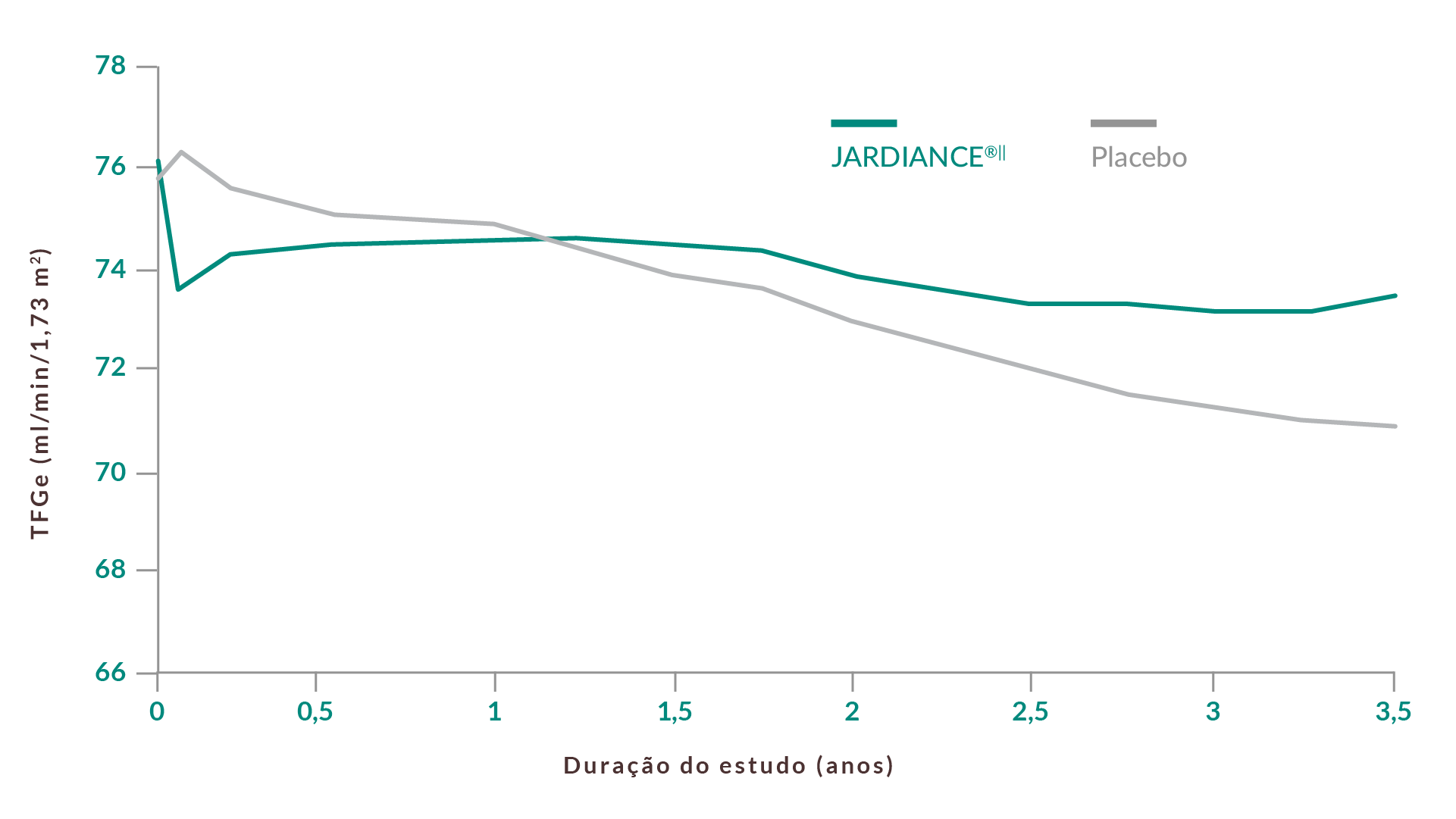
CONTEÚDOS RELACIONADOS

RECOMENDAÇÕES DAS GUIDELINES

RECOMENDAÇÕES DE DOSAGEM

PERFIL DE SEGURANÇA E TOLERABILIDADE
Indicações
JARDIANCE® está indicado para o tratamento de adultos e crianças com idade igual ou superior a 10 anos com diabetes mellitus tipo 2 insuficientemente controlados, como um adjuvante da dieta e do exercício
em monoterapia quando a metformina é considerada inapropriada devido à intolerância
em associação com outros medicamentos para o tratamento da diabetes
JARDIANCE® é indicado em adultos para o tratamento da insuficiência cardíaca crónica sintomática.
JARDIANCE® é indicado em adultos para o tratamento da doença renal crónica.
Notas de rodapé
-
§
Doentes adultos com DT2 insuficientemente controlada e DAC, DAP ou antecedentes de EM ou AVC.1,2
-
¶
A incidência ou agravamento de nefropatia é definida como a progressão para a macroalbuminúria, duplicação da creatinina sérica, uma TFGe ≤ 45 ml/min/1,73 m2; início de terapêutica de substituição renal; morte por doença renal. A incidência ou agravamento de nefropatia constituiu um componente pré-especificado do resultado microvascular secundário no ensaio EMPA-REG OUTCOME®. O resultado composto primário no estudo EMPA-REG OUTCOME® foi MACE de 3 critérios.2,3
-
#
O tratamento padrão incluiu medicamentos CV e agentes hipoglicemiantes administrados ao critério de profissionais de saúde e em conformidade com as recomendações presentes nas guidelines locais.1,2
-
||
Dados agrupados de doses de 10 mg e 25 mg de JARDIANCE®3
-
AVC = acidente vascular cerebral; CV = cardiovascular; DAC = doença arterial coronária; DAP = doença arterial periférica; DCVe = doença cardiovascular estabelecida; DT2 = diabetes tipo 2; EM= enfarte do miocárdio; MACE = acontecimentos cardiovasculares adversos major (major adverse cardiovascular events); RRR = redução do risco relativo; TFGe = taxa de filtração glomerular estimada.
Bibliografia
-
RCM de Jardiance® (Abr/2025)
-
Zinman B, Wanner C, Lachin JM, et al; EMPA-REG OUTCOME Investigators. Empagliflozin, cardiovascular outcomes, and mortality in type 2 diabetes. N Engl J Med. 2015;373(22):2117-2128. (EMPA-REG OUTCOME® results and the publication’s Supplementary Appendix.)
-
Wanner C, Inzucchi SE, Lachin JM, et al; EMPA-REG OUTCOME Investigators. Empagliflozin and progression of kidney disease in type 2 diabetes. N Engl J Med. 2016;375(4):323-334.
PC-PT-103910_agosto/2025
